Biohajoavia ortopedisia implantteja kehittävä Bioretec kertoi keskiviikkona, että sen RemeOs-traumaruuville on myönnetty Yhdysvaltain Centers for Medicare & Medicaid Services (CMS) toimesta Transitional Pass-Through (TPT) -korvattavuus lokakuun alkaen.
RemeO-traumaruuvi sai TPT-hyväksynnän vaihtoehtoisen väylän kautta, joka on tarkoitettu laitteille, joilla on sekä Breakthrough Device -status että FDA:n myyntilupa.
TPT-korvattavuus tarjoaa sairaaloille ja päiväkirurgisille yksiköille lisäkorvauksen uusista ja innovatiivisista teknologioista. Sen tarkoituksena on kattaa uusien ja innovatiivisten laitteiden lisäkustannus verrattuna olemassa oleviin hoitoihin. Korvattavuus madaltaa sairaaloiden kynnystä ottaa RemeOs-traumaruuvi käyttöön ja mahdollistaa sen tarjoamisen yhä laajemmalle potilasjoukolle.
Tällainen korvattavuus otetaan käyttöön silloin, kun tuote on hiljattain hyväksytty käyttöön, sen kustannus palveluun liittyen on merkittävä, ja sitä ei vielä sisällytetä vakiintuneisiin hoitopakoihin.
TPT -korvattavuus myönnetään yleensä kahdeksi tai kolmeksi vuodeksi, minkä aikana kerätään käyttötietoa korvausmallin tarkentamiseksi tulevaisuutta varten.
RemeOs-traumaruuvi on Yhdysvalloissa ensimmäinen ja ainoa osteopromotiivinen, biohajoava metallinen implantti ortopediseen käyttöön. steopromotiivinen tarkoittaa biologista ominaisuutta, jonka avulla materiaali tai tuote edistää uuden luukudoksen muodostumista ja kasvua elimistössä.
Bioretecin traumaruuvi on suunniteltu edistämään luutumista ja hajoamaan vähitellen korvautuen uudella luulla, mikä vähentää pysyvien implanttien riskejä ja kustannuksia.
Päätös TPT-korvattavuudesta seuraa RemeOs-traumaruuville maaliskuussa 2023 myönnettyä FDA:n De Novo -hyväksyntää ja tekee Bioretecistä yhden harvoista yhtiöistä, jotka ovat saaneet hyväksynnän sekä viranomaisilta että maksajilta läpimurtohoitoa edustavan teknologian kliinisestä ja taloudellisesta arvosta.
Kuluvan vuoden tammikuussa Bioretec saavutti merkittävän virstanpylvään, kun yhtiö sai CE-merkinnän traumaruuvin tuoteryhmälle EU:n lääkinnällisistä laitteista annetun asetuksen (MDR) mukaisesti.
Bioretecilla on vielä pitkä matka kannattavaan liiketoimintaan.
Huhti–kesäkuussa yhtiön liikevaihto laski lähes 51 prosenttia vertailukaudesta ja oli vain 0,67 miljoonaa euroa. Toisen vuosineljänneksen liikevaihtoon vaikuttivat Spartan Medicalin Yhdysvaltojen pilottijakelusopimuksen päättymiseen liittyvä kertaluonteinen hyvityslasku ja muutos jakelukumppaniverkostossa.
Lisäksi vertailukausi sisälsi suuren aloitustoimituksen uudelle jakelijalle. Myynti varastoiville jakelijoille on epätasaista, mikä voi aiheuttaa vuosineljänneskohtaista vaihtelua liikevaihdossa.
Koko alkuvuonna tammi–kesäkuun liikevaihto pysyi odotetusti vakaana ja oli 2,06 miljoonaa euroa, mikä vastaa edellisvuoden lukemia.
Myyntikate (ilman muita tuottoja) huhti–kesäkuussa oli 0,19 miljoonaa euroa Myyntikatteeseen vaikuttivat myyntitoimitusten jatkuminen Kiinaan, missä marginaalit ovat hieman alhaisemmat, sekä materiaali- ja palvelukustannusten kasvu, mikä liittyi muutokseen jakelukumppaniverkostossa.
Yhtiö odottaa markkinakehitys- ja skaalausvaiheiden myyntikatteen paranevan myynnin kasvaessa ja kun suorajakelukumppanit vakiintuvat.
Huhti-kesäkuun tappio oli -3,5 miljoonaa euroa.
Bioretec Oy järjesti viime kesäkuussa merkintäetuoikeusannin, joka ylimerkittiin. Yhtiö sai osakeannista noin 9,2 miljoonan euron bruttotuotot.
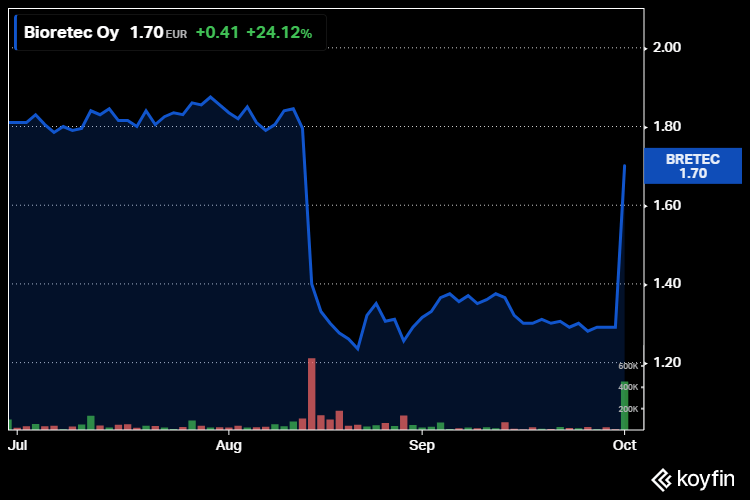
TPT-päätös oli mannaa markkinoille. Bioretecin osake lähti heti yhtiön tiedotteen jälkeen jyrkkään nousuun ja päätyi keskiviikkona lähes 32 prosentin nousuun. Vuoden alusta osake on kuitenkin edelleen laskenut 25 prosenttia.